Entropi, S
Tenaga yang berkaitan dengan darjah kecelaruan. Semakin bercelaru sesuatu sistem, semakin tinggi entropi sistem tersebut. Perubahan ke arah lebih bercelaru adalah perubahan yang lebih cenderung berlaku. Keadaan yang lebih bercelaru adalah keadaan yang lebih cenderung tercapat.
Contoh-contoh perubahan dengan DS positif.
1. Pengembangan gas
2. Penaikan suhu
3. Perubahan fasa daripada fasa yang lebih terkondensasi kepada fasa yang kurang terkondensasi:
Pepejal ¾® Cecair (peleburan)
Cecair ¾® Gas (pendidihan)
Pepejal ¾® Gas (pemejalwapan)
4. Kekompleksan molekul
H2(g) ¾® 2H(g) (pengatoman)
Takrif:
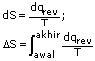
Penilaian berangka memerlukan korelasi diantara dq dengan T.
Contoh 1: Perubahan Fasa
Proses berlaku dengan pemindahan haba pendam (latent heat) pada suhu tetap
Dalam proses ini, 
Contoh 2: Pengembangan isotermal (T tetap) gas unggul, PV = nRT.
Bermula dengan,
DE = q + w
Pada suhu tetap, DT = 0
Mengikut persamaan kinetik, DE = 0, oleh itu, q = -w, dan dq = -dw
Bagi gas unggul ini, 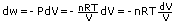

Dalam sebutan tekanan P, 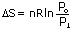
Asalnya entropi diterbitkan daripada wacana statistik.
Pengembangan entropi menghasilkan Hukum Termodinamik 2, HT2:
Dalam proses spontan, perubahan entropi semesta adalah positif, dan sebaliknya bagi proses tak spontan.
DSsemesta = DSsistem + DSsekitar
Bagi 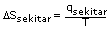
qsekitar = -qsistem
Oleh itu 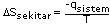
Pada T dan P tetap, qsistem = DHsistem
Dengan demikian, 
Penyusunan semula: -TDSsemesta = DHsistem - TDSsistem
DSsemesta bernilai positif untuk perubahan spontan,
Dengan demikian, -TDSsemesta bernilai negatif untuk perubahan spontan,
Ia itu, ungkapan DHsistem - TDSsistem bernilai negatif.
Hukum Termodinamik 3, HT3
Pada suhu 0 K, entropi jirim berhablur sempurna adalah sifar. Hukum ini membolehkan penghitungan entropi mutlak sesuatu jirim.
Hukum Termodinamik 0, HT0
Jika jirim A yang bersuhu T kelvin bersentuhan dengan jirim B sehingga keseimbangan terma tercapai, maka jirim B juga bersuhu T kelvin. Hukum ini membolehkan suhu sesuatu jirim disukat dengan menggunakan termometer.
Tenaga Bebas Gibbs, G
Daripada hujah entropi semesta,
-TDSsemesta = DHsistem - TDSsistem
Ditakrifkan: [DG]sistem = [DH - TDS]sistem
Proses spontan berlaku apabila DG bernilai negatif.
Persamaan ini menyimpulkan situasi tertentu di mana proses spontan berlaku bagi kes-kes yang perubahan entalpinya DH positif, dan kes-kes yang perubahan entropinya DS negatif.
Peranan Suhu
DG = DH - TDS
Suhu memainkan peranan dalam penentuan tanda DG kerana sebutan DH dan TDS berlawanan tanda.
| DH | DS | DG | Contoh |
| (-) | (+) | DG (-) pada sebarang suhu | Proses semula jadi seperti peruntuhan banggunan, pengaratan besi, penuaan benda-benda hidup. |
| (-) | (-) | DG (-) pada suhu rendah | Pembekuan air: H2O(c) ¾® H2O(p) |
| (+) | (+) | DG (-) pada suhu tinggi | Peleburan air: H2O(p) ¾® H2O(c) |
| (+) | (-) | DG (+) pada semua suhu. Perubahan tidak spontan | ::Air mendaki bukit. ::Banggunan terbina secara sendiri daripada batu-bata. |