Persamaan Maxwell
Korelasi antara kuantiti-kuantiti termodinamik.
| mnemonic device | 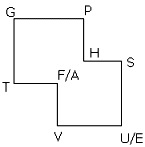 | Good Physicalchemist Have Studied Under Very Fine Teachers |
Contoh penerbitan.
G berfungsikan P dan -T.
dG = VdP - SdT
Memberikan: 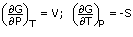
Sehingga kerbedaan penuh menjadi: 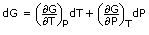
Fungsi-fungsi untuk H(P,S), E(S,-V), dan A(-T,-V) boleh diterbitkan dengan cara yang serupa.
Kuantiti Separa Molar
Nilai intensif sifat termodinamik.
Sifat termodinamik:
Isipadu, V
Suhu, T
Tekanan, P
Entalpi, H
Tenaga dalaman, E (U)
Entropi, S
Tenaga bebas Gibbs, G
Tenaga bebas Helmhotz, A (F)
Amaun, mol, n
Persamaan Keadaan Umum: Q = f(V, T, P, ..., n1, n2, ...)
Kuantiti separa molar ditakrifkan sebagai: 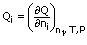
Jadi perubahan penuh kuantiti dQ adalah

Contohnya,
Isipadu separa molar: dV = V1dn1 + V2dn2 + ... + Vidni
Vi = isipadu separa molar komponen-i.
Tenaga bebas separa molar: dG = G1dn1 + G2dn2 + ... + Gidni
Gi = tenaga bebas separa molar komponen-i.
Keupayaan Kimia, m
Nama khusus bagi tenaga bebas separa molar, 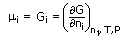
Dengan demikian, dG = m1dn1 + m2dn2 + ... + midni = åmidni (pada P dan T tetap).
Mengaplikasikan persamaan Maxwell, G = f(T, P, ni),
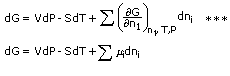
Juga dengan tenaga lain, misalnya, entalpi, H = f(P, S, ni)
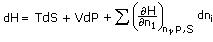
Daripada G = H - TS; dG = dH - Tds - SdT
Menggantikan dH,
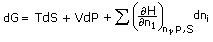 - Tds - SdT
- Tds - SdT
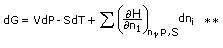
Perbandingan persamaan ** dengan persamaan *** memberikan,

Dengan cara yang serupa kita boleh menerbitkan ungkapan untuk keupayaan kimia dalam sebutan tenaga-tenaga lain.

Korelasi-korelasi ini menggambarkan bagaimana tenaga-tenaga temodinamik berubah apabila keupayaan kimia berubah.
Keseimbangan dan Tenaga Bebas Gibbs
DG = DH - TDS
Misalkan suatu gas unggul, dengan persamaan keadaannya, PV = nRT; P = nRT/V.
Misalkan perubahan berlaku kepada gas ini, iaitu pengembangan pada suhu tetap T daripada berisipadu V1 kepada berisipadu V2.
Bagi proses ini DH = 0, kerana DT = 0.
Cuma DS berubah: 
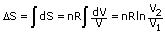
Dengan demikian,

Sebutan V1/V2 atau P2/P1 adalah nilai yang berkaitan dengan keadaan akhir sistem relatif kepada keadaan awal sistem tersebut; atau sebaliknya.
Namakan sebutan ini Q', dengan demikian DG = nRTlnQ'
Tenaga bebas Gibbs tidak boleh ditentukan secara mutlak. Keadaan piawai dipilih (juga untuk tenaga-tenaga lain, kecuali entropi, S).
Pada keadaan piawai ini, misalkan sebutan V1/V2 atau P2/P1 bernilai Qo.
Jadi pada keadaan piawai, DGo = nRTlnQo
Dengan hujah kerelatifan yang serupa, pada keadaan tidak piawai, korelasi berikut berlaku:
DG - DGo = nRTlnQ' - nRTlnQo

Dengan Q = Q'/Qo merupakan kuantiti yang berkaitan dengan keadaan awal, keadaan akhir dan keadaan piawai.
Bagi perubahan kimia, yang melibatkan perubahan bilangan zarah setelah tindak balas selesai, persamaan boleh diubahsuai menjadi,
DG = DGo + RTlnQn
Sebutan Qn adalah berkorelasi dengan pemalar keseimbangan, K, sehingga,
DG = DGo + RTlnK