Pencampuran merupakan satu proses. Proses ini spontan jika hasil pencampuran mempunyai tenaga bebas Gibbs yang lebih rendah.
Misalkan pencampuran nA mol gas unggul A dengan nB mol gas unggul B.
Jumlah mol, n = nA + nB

Pada keadaan awal, keupayaan kimia,
Bagi komponen A: 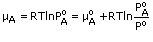
Bagi komponen B: 
Tenaga bebas jumlah sistem, Gi = nAµA + nBµB
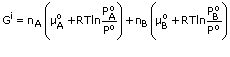
Selepas pencampuran, tekanan separa A menjadi PA dan tekanan separa B menjadi PB; tenaga bebas tersebut menjadi,
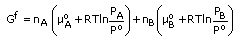
Perubahan tenaga bebas pencampuran DGm = DGf - DGi
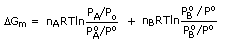
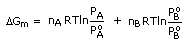
Mengaplikasikan hukum Dalton dan hukum Raoult: xA = PA/PAo; xB = PB/PBo
DGm = nARTlnxA + nBRTlnxB = RT(nAlnxA + nBlnxB) = RTånilnxi
DGm = nRT(xAlnxA + xBlnxB) = nRTåxilnxi
Ciri-ciri persamaan:
x - pecahan
lnx - negatif
xlnx - negatif
nRT - selalu positif
DGm - selalu negatif (spontan - untuk pencampuran gas unggul
DGm - berkadar terus kepada T
DGm - bebas daripada tekanan jumlah P
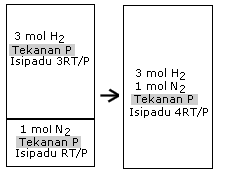
[Atkins & Paula, Hlm 167, Eg 7.2]. 3 mol hidrogen H2 dicampurkan dengan 1 mol nitrogen N2 pada suhu 298 K pada tekanan yang sama. Anggap hidrogen dan nitrogen berkelakuan unggul, hitung perubahan tenaga bebas pencampuran tersebut. [R = 8.314 JK-1mol-1; pada 298 K, RT298 = 8.314 x 298 = 2.5 kJ mol-1]. Proses 1
Penyelesaian
|
DGm = nARTlnxA + nBRTlnxB = RT(nAlnxA + nBlnxB) n(H2) = 3 mol n(N2) = 1 mol x(H2) = 3/4 = 0.75; lnx(H2) = - 0.2877 x(N2) = 1/4 = 0.25; lnx(N2) = - 1.3863 DGm = (2.5){3(-0.2877) + (1)(-1.3863)} = -5.62 kJ |
 |
Nota:
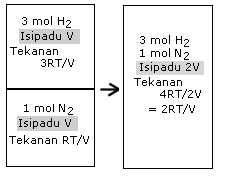
Sebelum pencampuran: Isipadu H2 = 3RT/P; Isipadu N2 = RT/P; Isipadu jumlah = 4RT/P.
Selepas pencampuran: Isipadu = (3+1)RT/P = 4RT/P.
Penghitungan Terperinci
Pencampuran dilakukan pada tekanan yang sama, P; anggap keadaan piawai yang sama Po.
Sebelum bercampur: G(H2) = Go + 3RTln(P/Po); G(N2) = Go + RTln(P/Po)
Gawal = G(H2) + G(N2) = 2Go + 4RTln(P/Po)
Selepas bercampur: G(H2) = Go + 3RTln(¾P/Po); G(N2) = Go + RTln(¼P/Po)
Gakhir = 2Go + 3RTln(¾P/Po) + RTln(¼P/Po)
DGm = Gakhir - Gawal
= 3RTln(¾P/Po) + RTln(¼P/Po) - 4RTln(P/Po)
= 3RTln¾ + 3RTln(P/Po) + RTln¼ + RTln(P/Po) - 4RTln(P/Po)
= 3RTln¾ + RTln¼
= (3)(2.5)(-0.2877) + (2.5)(-1.3863)
= -5.62 kJ
Jika pencampuran dilakukan daripada keadaan awal yang berlainan, misalnya (Proses 2) pada isipadu sama V, maka DGm yang berlainan nilai diperoleh. Misalnya:
|
|
Sebelum bercampur: G(H2) = Go + 3RTln(3RT/V) - 3RTlnPo G(N2) = Go + RTln(RT/V) - RTlnPo Gawal = G(H2) + G(N2) = 2Go + 3RTln(3RT/V) + RTln(RT/V) - 4RTlnPo = 2Go + 3RTln3 + 4RTln(RT/V) - 4RTlnPo Selepas bercampur: G(H2) = Go + 3RTln{(3/4)(2RT/V)} - 3RTlnPo = Go + 3RTln(3/2) + 3RTln(RT/V) - 3RTlnPo G(N2) = Go + RTln{(1/4)(2RT/V)} - RTlnPo = Go + RTln(1/2) + RTln(RT/V) - RTlnPo Gakhir = G(H2) + G(N2) = 2Go + 3RTln(3/2) + RTln(1/2) + 4RTln(RT/V) - 4RTlnPo |
DGm = Gakhir - Gawal
= [2Go + 3RTln(3/2) + RTln(1/2) + 4RTln(RT/V) - 4RTlnPo] - [2Go + 3RTln3 + 4RTln(RT/V) - 4RTlnPo]
= 3RTln(3/2) + RTln(1/2) - 3RTln3 = 4RTln(1/2)
= 4RTln(1/2)
= (4)(2.5 kJ mol-1)(-0.6932) = -6.93 kJ
Perbezaan DGm - Proses 2 vs Proses 1 - sebesar (-6.93) - (5.62) = -1.31 kJ adalah disebabkan oleh perbezaan perubahan tekanan.