Larutan
Larutan adalah sejenis campuran. Ia merupakan sistem yang terdiri daripada dua atau lebih komponen yang berkeseimbangan dalam satu fasa sahaja. Kita biasanya menamakan komponen yang lebih kecil sebagai bahan larut, manakala komponen yang lebih besar sebagai pelarut. Namun begitu, oleh sebab setiap komponen mempunyai fasa wap masing-masing, maka larutan ringkas adalah sistem 2-komponen 2-fasa (sistem BIVARIAN).
|
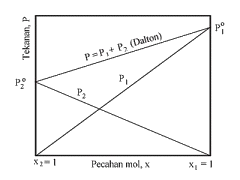
Korelasi termodinamik yang paling ringkas mengenai larutan ialah Hukum Raoult: P1 = x1P1o dan P2 = x2P2o; dengan xi ialah pecahan mol komponen-i dan Pio ialah tekanan wap komponen-i tulen. Dengan notasi lain, jika a adalah fasa cecair, dan b adalah fasa wap bagi larutan berkenaan, maka bagi komponen-i: Jika fasa wap (fasa b) berkelakuan gas unggul, maka dengan pegolahan µib, bentuk lain persamaan Raoult terhasil: dengan |
 |
Apabila kita memerihal sesuatu larutan, biasanya keupayaan kimia komponen-i di dalam larutan yang diperkatakan, jadi superskrip a digugurkan, menjadikan persamaan Raoult:
Bagi sistem gas, sebutan Pi/Pio mempunyai kaitan dengan fugasiti, dan seterusnya berkaitan dengan aktiviti. Secara ringkas, bagi sistem unggul, persamaan Raoult adalah:
Larutan Unggul
ISIPADU
Bagi sistem unggul, mengikut Raoult:
Dari segi isipadu,
maka (¶m1/¶P)T,nj = V1 - isipadu separa molar komponen-1
Jadi, apabila kita membuat campuran, perubahan keupayaan kimia komponen-i adalah:
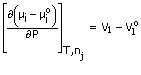
Daripada takrif keupayaan kimia, µi = µio + RTlnai = µio + RTlnxi,
maka, µi - µio = RTlnai = RTlnxi
dan ¶(µi - µio) = RT¶lnai = RT¶lnxi
Jadi, bagi pencampuran unggul,
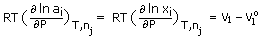
Oleh sebab  , maka
, maka 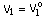
Dengan perkataan, isipadu separa molar komponen-i dalam campuran unggul, adalah sama dengan isipadu molar komponen-i tulen. Apabila berlaku pencampuran unggul, isipadu jumlah campuran adalah hasil tambah isipadu masing-masing komponen.
ENTALPI
Daripada persamaan Gibbs-Helmholtz: 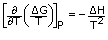 ,
,
serta operasi kalkulus standard, (-1/T2)dT = d(1/T),
dan persamaan Raoult bagi keupayaan kimia, µi - µio = RTlnai = RTlnxi,
maka, entalpi separa molar komponen-i.
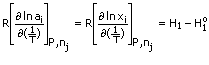
Oleh sebab sebutan ¶lnxi = 0, maka H1 - H1o = 0, iaitu H1 = H1o
Dengan perkataan, entalpi separa molar komponen-i dalam larutan unggul adalah sama dengan entalpi separa molar tulennya, iaitu perubahan entalpi adalah sifar dalam pencampuran unggul.
TENAGA BEBAS GIBBS
Perubahan tenaga bebas Gibbs tidak boleh sifar dalm pencampuran (pelarutan) unggul, kerana proses ini adalah proses spontan. Sebaliknya, perubahan tenaga bebas Gibbs, DG mestilah negatif.
Bagi pencampuran DGm adalah:
Daripada µi = µio + RTlnai = µio + RTlnxi
maka, DGm = G - Go = RTånilnai = RTånilnxi
Bagi campuran unggul dua komponen (larutan unggul ringkas),
ENTROPI
Entropi juga tidak sifar dalam pencampuran. Sebaliknya entropi bertambah.
Perbandingan persamaan DGm = RTånilnai = RTånilnxi
dengan persamaan DGm = DH - TDSm, dengan DHm = 0 bagi pencampuran unggul, maka terhasillah entropi pencampuran unggul,
Bagi campuran unggul dua komponen (larutan unggul ringkas),
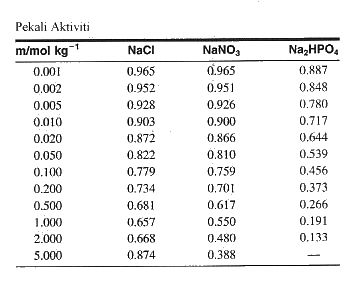
Aktiviti Pelarut dan Bahan Larut
Keupayaan kimia bahan larut diberikan oleh: µ2 = µ2o + RTlna2
Bagi larutan unggul: µ2id = µ2o + RTlnx2.
Penolakan menghasilkan µ2 - µ2id = RTln(a2/x2)
Takrifkan pekali aktiviti f2 = a2/x2, i.e. a2 = f2x2.
Dengan demikian f2 ® 1 apabila x2 ® 1.
|
Secara lain larutan unggul boleh ditakrifkan dalam sebutan kemolalan - mol kg-1 - sebagai: µ2id = µ2o + RTlnm2 Dengan cara penolakan yang sama, µ2 - µ2id = RTln(a2/m2) Di sini pekali aktiviti ditakrifkan sebagai g2 = a2/m2, i.e. a2 = g2m2.Dengan demikian, Dengan demikian g2 ® 1 apabila m2 ® 0. |
|